Biomarker-related phospho-tau217 appears in synapses around Aβ plaques prior to tau tangle in cerebral cortex of preclinical Alzheimer's disease
Cell Reports 44, 116203 | September 23, 2025 | DOI: 10.1016/j.celrep.2025.116203
시냅스 내 p-tau217 출현
preclinical AD 뇌의 Aβ plaque 주변 시냅스에서 p-tau217이 NFT 형성 이전에 puncta로 나타남
능동적 인산화 반응
p-tau217 양성 시냅스에 GSK3β, Cdk5, JNK 등 활성 tau kinase가 풍부하게 공존
신경/시냅스 반응의 지표
p-tau217은 글리아 세포에 의한 engulfment가 아닌, Aβ 병리에 대한 뉴런/시냅스 반응을 반영
p-tau217은 정상 뇌에는 없지만 preclinical AD에서 Aβ plaque 주변 pre/post-시냅스에 출현하며, tau tangle(NFT) 형성보다 선행한다. 이는 혈액 바이오마커 p-tau217이 Aβ 병리에 대한 초기 시냅스 반응을 반영함을 시사한다.
이 논문이 강한 임팩트를 가지는 이유: 아밀로이드 양/음성 판정에 뛰어난 성능을 보이는 p-tau217 바이오마커가 왜, 어디서, 어떻게 만들어지는지를 부검 뇌 조직에서 처음으로 규명했기 때문이다 — Aβ plaque 주변 시냅스에서 활성 kinase가 tau를 능동적으로 인산화하고 있었다.
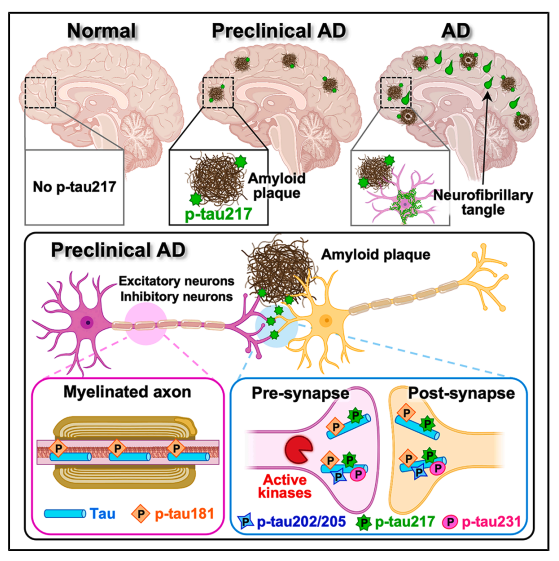
Background
논문 Introduction의 논리 흐름을 따라 — 왜 이 연구가 필요했는가
알츠하이머병과 조기 진단의 숙제
AD는 노인성 치매의 주요 원인이 되는 진행성 신경퇴행 질환이다. 병리학적으로 세 가지가 동시에 관찰된다: Aβ peptide로 구성된 senile plaque, 과인산화된 tau가 축적된 neurofibrillary tangle(NFT), 그리고 뇌 위축.
Aβ 축적은 임상 증상 발현 20년 이상 전부터 시작되며, 만성 신경염증·NFT 전파·뉴런 손실을 유발한다. 최근 항-Aβ 면역요법(lecanemab 등)이 승인되면서 plaque burden을 줄이고 인지 저하를 부분적으로 늦출 수 있게 되었지만, 치료 효과를 극대화하려면 preclinical 단계의 환자를 조기에 찾아내는 것이 핵심 과제가 되었다.
그렇다면 preclinical 단계를 어떻게 검출할 것인가?
표준 검사법의 벽
PET imaging은 살아있는 환자의 뇌에서 Aβ와 tau 병리를 검출할 수 있는 유일한 in vivo 방법이다. PET 연구가 밝혀낸 핵심은 Aβ는 임상 발현 20년 전부터, tau는 임상 발현 시점과 거의 동시에 검출된다는 시간적 비대칭이다.
그러나 PET 이미징은 고비용, 방사선 노출, 낮은 접근성, 환자 적용의 제한이라는 실질적 벽에 부딪힌다. 대규모 스크리닝이나 반복 측정에는 부적합하기 때문에, 면역요법 대상 환자를 효율적으로 발굴하려면 더 싸고 쉬운 대체 검사법이 필요했다.
더 싸고 쉽고 민감한 방법이 있어야 한다.
20-year window — 혈액으로 잡아낸 조기 신호
CSF 기반 p-tau 측정이 먼저 개발되었고, 이후 혈액 기반으로 확장되었다. p-tau181, p-tau205, p-tau217, p-tau231 등 서로 다른 인산화 부위가 모두 AD 환자에서 상승하지만, 그중 p-tau217이 가장 민감한 혈액 바이오마커로 자리 잡았다.
가장 중요한 발견은 이것이다: 혈중 p-tau217 상승은 Aβ PET 양성과 상관하며, tau PET이 양성이 되기 약 20년 전부터 검출된다. 즉 preclinical 단계의 뇌에서 이미 비정상적 tau 인산화가 일어나고 있으며, 혈중 p-tau217은 Aβ plaque 형성과 관련된 초기 신경병리학적 변화를 반영한다는 것을 시사한다.
본 그림은 논문 본문(Jack et al., 2013; Palmqvist et al., 2020 등)의 시점 보고를 바탕으로 한 개념도이며, 각 바이오마커의 시작/상승 시점은 개인차가 크고 수치는 근사치이다.
정확한 시점은 개인차가 있지만, 평균적으로 혈중 p-tau217은 tau PET보다 수년~수십년 이르다.
답하지 못한 두 질문
Gap A · 공간 정보의 부재
혈액·CSF 바이오마커는 "뇌 어딘가에서 p-tau217이 나오고 있다"는 것만 알려준다. 어느 뇌 영역, 어떤 세포 유형, 어떤 세포소기관에서 생성되는지는 체액 샘플만으로는 알 수 없다. 신경병리학적 맥락이 없는 상태에서 바이오마커를 해석하는 것은 불완전하다.
Gap B · 풀리지 않은 미스터리 ★
선행 부검 연구는 AD 환자 뇌에서 p-tau217이 주로 NFT·pretangle·GVD(granulovacuolar degeneration body)에서 검출됨을 보였다 — 즉 tau 전파와 연결되는 듯했다. 그런데 preclinical 단계에서는 혈중 p-tau217이 tau 병리가 아닌 Aβ PET 양성과 강하게 상관한다. 왜 preclinical p-tau217은 tau가 아닌 Aβ 병리를 예측하는가? — 이것이 이 논문의 핵심 연구 질문이다.
preclinical 뇌 조직을 직접 들여다봐야 답이 나온다.
3가지 구체적 질문으로 좁힌 스코프
부위 선택: Middle frontal gyrus의 frontal cortex(FC)를 선택했다. 이 영역은 Aβ plaque가 NFT보다 앞서 형성되는 곳이므로, preclinical 단계의 가장 이른 p-tau217 신호를 잡아내기에 최적이다.
어디에 나타나는가
p-tau217은 Aβ plaque와 어떤 공간적 관계를 갖고, 다른 phospho-site(181/205/231/262)와 함께 나타나는가?
어떤 구조물·세포에서
축삭인가 시냅스인가? 흥분성 뉴런인가 억제성 뉴런인가? 글리아가 engulf한 잔해인가?
어떻게 만들어지는가
현장에 활성 tau kinase(GSK3β, Cdk5, JNK)가 존재하는가? 능동적 인산화의 증거가 있는가?
Methods
부검 뇌 조직 기반 면역조직화학 및 초해상도 현미경 분석
Postmortem Brain Cohort
총 34명의 부검 뇌 샘플을 사용하였다. 뇌 조직은 두 기관의 Brain Bank에서 제공받았다: Brain Bank for Aging Research(Tokyo Metropolitan Institute for Geriatrics and Gerontology)와 NCNP Brain Bank(National Center of Neurology and Psychiatry). 분석 부위는 middle frontal gyrus의 frontal cortex(FC) 절편이다.
SP 0, NFT 0-2
남 6 / 여 9
SP 1-2, NFT 0-3
남 5 / 여 4
SP 3, NFT 3-6
남 5 / 여 5
Control 그룹은 CN 대상자로 구성되며, Preclinical AD 그룹에 CN과 MCI 대상자가 함께 포함된다. 모든 대상자에 대해 Braak SP stage와 NFT stage가 평가되었으며, CDR은 0~0.5이다. 대상자별 상세 정보는 논문 Table S1에 기재되어 있다.
Results I: p-tau217의 시공간적 출현
Aβ plaque 주변에 p-tau217 puncta가 NFT 이전에 나타난다
정상 뇌에서는 부재
Control(Aβ-/NFT-) 뇌에서 p-tau217 신호와 Aβ 신호 모두 관찰되지 않았다.
preclinical AD에서 출현
Preclinical AD(Aβ+/NFT-) 뇌에서 Aβ plaque 주변에 p-tau217 양성 puncta가 pretangle이나 NFT 없이도 출현. Diffuse 및 dense-core plaque 모두에서 관찰.
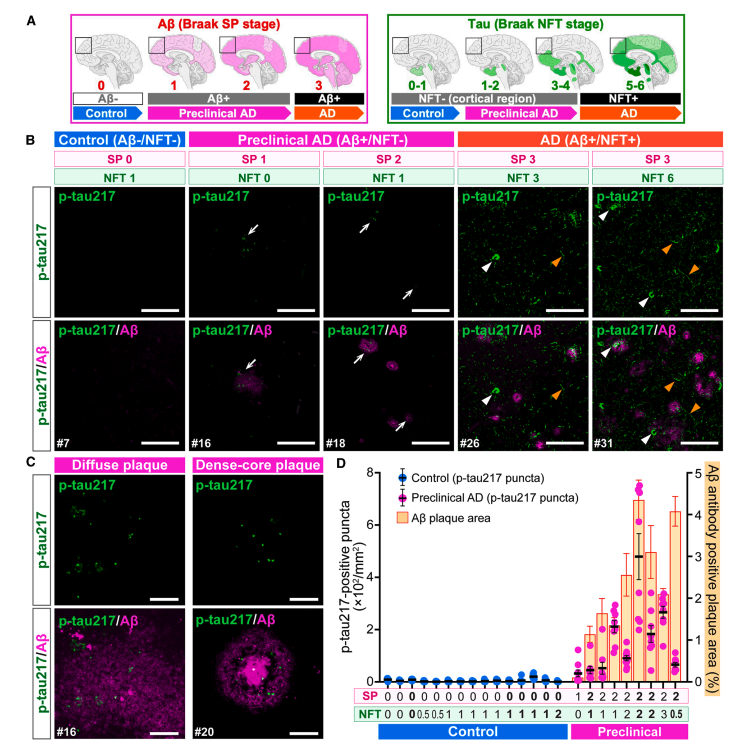
AD, Alzheimer's disease; Aβ, amyloid-β; SP, senile plaque; NFT, neurofibrillary tangle; NT, neuropil thread; FC, frontal cortex. 클릭하여 확대
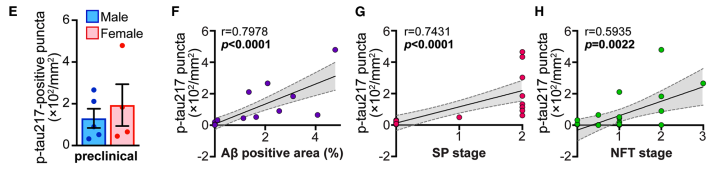
SP, senile plaque; NFT, neurofibrillary tangle. 클릭하여 확대
Figure 1 간단 요약: 이 그림이 왜 중요한가?
기존 상식: 혈액/CSF에서 p-tau217 수치가 올라가면 뇌에 Aβ가 쌓이고 있다는 뜻이라는 건 알려져 있었다. 뇌 조직에서도 NFT, pretangle, granulovacuolar degeneration body 등 이미 병리가 진행된 구조물에서 p-tau217이 검출된 적은 있었다. 하지만 preclinical AD 뇌에서 Aβ plaque 주변에 p-tau217이 NFT와 독립적으로 나타나는지를 체계적으로 확인한 연구는 없었다.
이 Figure가 보여주는 것: p-tau217은 정상 뇌에는 전혀 없고, Aβ plaque가 생기는 순간부터 그 주변에 puncta 형태로 나타난다. 중요한 건 이 시점에 NFT는 아직 없다는 것이다. 즉, p-tau217은 tau tangle의 부산물이 아니라, Aβ plaque에 대한 독립적인 초기 반응이다. 다만 이 puncta가 정확히 어떤 구조물 안에 있는지 — axon인지 synapse인지 — 는 Figure 1만으로는 알 수 없으며, Figure 3-4에서 synapse marker 공염색을 통해 규명된다.
Amyloid PET 양성이지만 tau PET 음성인 환자에서 혈장 p-tau217이 올라가는 이유의 첫 단서를 제공한다. tau PET이 잡는 NFT와는 독립적으로, plaque 주변에서 별개의 p-tau217 생성이 일어나고 있기 때문이다.
Aβ plaque 주변에 p-tau217만 있는 건가? 다른 p-tau도 함께 나타나는가?
알아두면 좋을 것: p-tau의 종류 — 181, 202/205, 217, 231은 뭐가 다른가?
Tau 단백질(441개 아미노산)에는 인산화될 수 있는 부위가 수십 개 있다. 각 부위의 번호가 곧 바이오마커 이름이 된다. 이 논문에서 다루는 주요 p-tau 종은 다음과 같다:
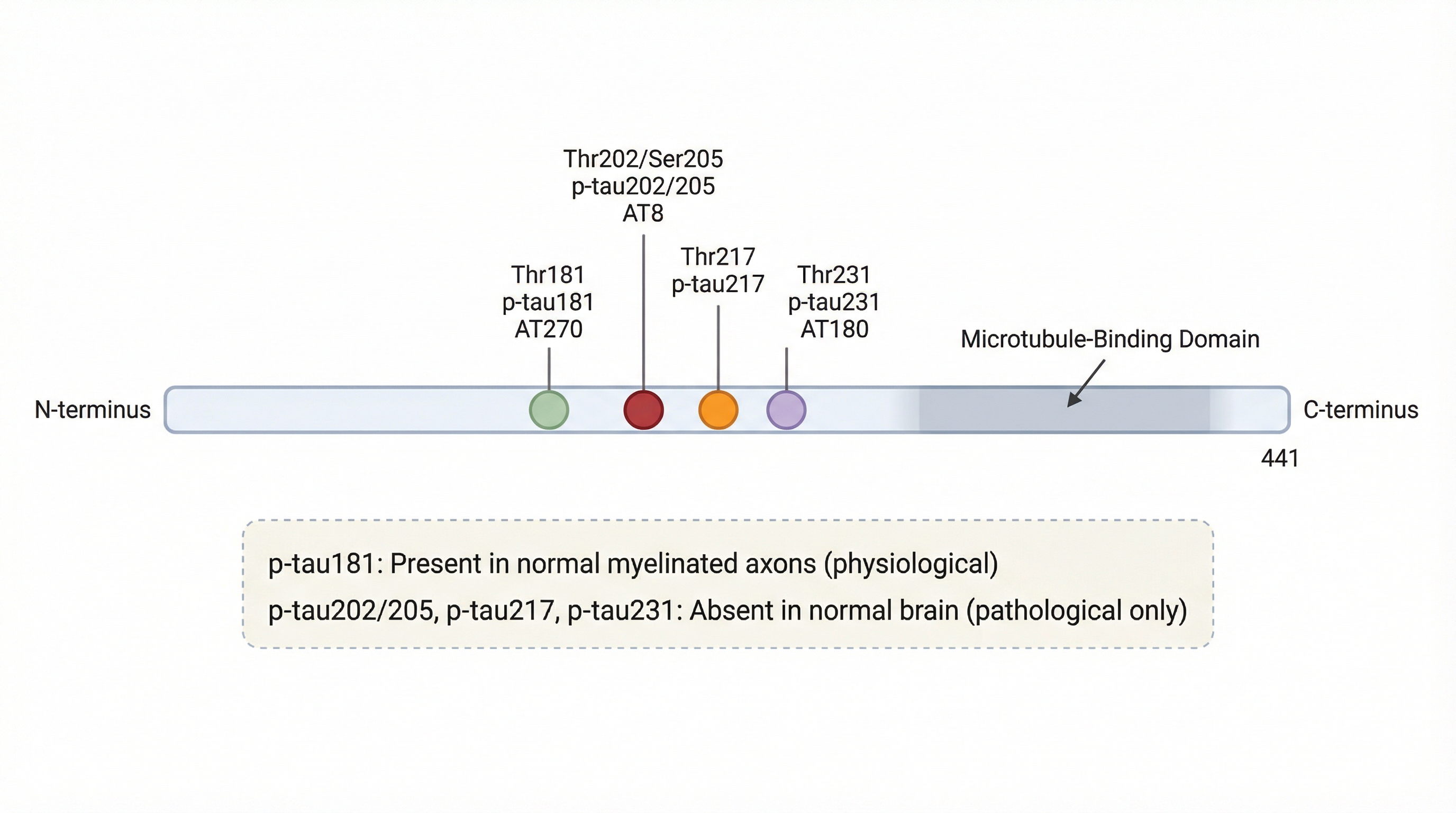
p-tau181 — 정상 뇌의 myelinated axon에도 존재하는 유일한 생리적 인산화. CSF 바이오마커로 오래 사용됐으나, 정상에서도 기저 수준이 있어 특이도가 상대적으로 낮다. 이 논문에서는 축삭 손상의 지표로 해석.
p-tau202/205 — 정상 뇌에 없음. NFT와 pretangle의 대표 마커. "tau 병리 = AT8 양성"이라고 할 정도로 널리 쓰임.
p-tau217 — 정상 뇌에 없음. 이 논문의 주인공. preclinical AD에서 가장 민감한 혈액 바이오마커. Aβ plaque 주변 시냅스에서 능동적으로 생성.
p-tau231 — 정상 뇌에 없음. 역시 혈액/CSF 바이오마커. p-tau217과 Aβ plaque 주변에서 ~80-92% 공존.
알아두면 좋을 것: Aβ plaque 성숙 단계와 Thioflavin-S(ThS)
Aβ plaque는 시간에 따라 성숙한다. 초기에는 Aβ 펩타이드가 느슨하게 퍼진 diffuse plaque로 시작하여, 응집이 진행되면 조밀한 아밀로이드 코어를 가진 dense-core plaque가 되고, 최종적으로 주변에 손상된 신경돌기와 활성화된 글리아가 모여드는 neuritic plaque로 발전한다.

Thioflavin-S(ThS)는 β-sheet 구조에 결합하여 형광을 내는 염색 시약이다. Dense-core 이상의 성숙 plaque는 β-sheet 구조를 갖추므로 ThS 양성이 되고, diffuse plaque는 ThS 음성일 수 있다. 이 섹션의 실험에서는 ThS 양성 Aβ plaque(= 성숙한 plaque) 주변에서 p-tau217과 다른 p-tau 종의 공존을 분석하였다.
AT8(p-tau202/205)과의 관계
AT8은 tau의 202/205번 부위 인산화를 인식하는 항체로, tau 병리의 대표적 마커이다. 연구진은 ThS 양성(= 성숙한 β-sheet 구조를 가진) Aβ plaque 주변에서 p-tau217과 AT8을 동시에 염색하여, preclinical AD 뇌에서 두 신호가 같은 위치에 나타나는지 확인했다. 결과적으로, p-tau217 puncta의 약 70%가 AT8 puncta와 겹쳤고, 반대로 AT8 puncta의 약 85%가 p-tau217과 겹쳤다. 이는 Aβ plaque 주변에서 tau의 여러 부위가 동시에 인산화됨을 의미한다.
p-tau231과의 공존
p-tau231은 tau의 231번 부위 인산화를 의미하며, 역시 AD의 혈액/CSF 바이오마커로 쓰인다. 연구진은 ThS 양성 Aβ plaque 주변에서 p-tau217과 p-tau231을 동시에 염색했다. 그 결과, p-tau217 puncta의 80.4%가 p-tau231과 겹쳤고, p-tau231 puncta의 92.1%가 p-tau217과 겹쳤다. 즉, Aβ plaque 주변 시냅스에서 tau의 217번과 231번 부위가 거의 함께 인산화되고 있다는 뜻이다.
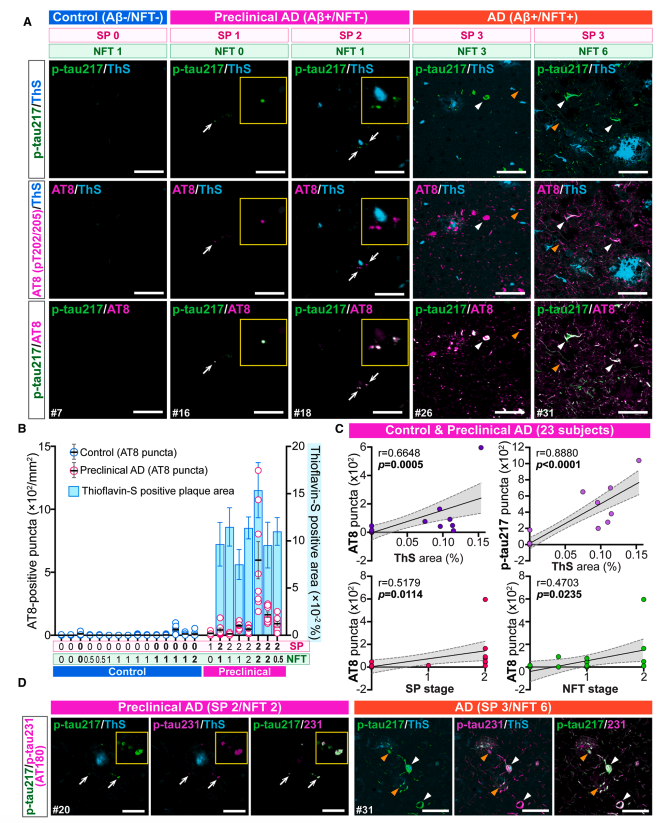
ThS, Thioflavin-S; AT8, anti-p-tau202/205 antibody; NT, neuropil thread; NFT, neurofibrillary tangle; SP, senile plaque. 클릭하여 확대
Figure 2 간단 요약: 이 그림이 왜 중요한가?
Figure 1에서 남은 질문: p-tau217이 Aβ plaque 주변에 나타난다는 걸 봤다. 그런데 tau에는 인산화 부위가 수십 개 있다. p-tau217만 나타나는 건가, 아니면 다른 부위도 동시에 인산화되는 건가?
이 Figure가 보여주는 것: Aβ plaque 주변에서 p-tau217은 혼자가 아니다. AT8(p-tau202/205)과 ~70-85%, p-tau231과 ~80-92% 겹친다. 즉, Aβ plaque 주변에서 tau의 여러 부위가 동시에 인산화되고 있다. 이건 단순한 우연이 아니라 체계적인 반응이다.
혈액/CSF에서 p-tau217, p-tau181, p-tau231 수치가 각각 측정되는데, 이들이 뇌 조직에서 같은 곳(Aβ plaque 주변)에서 함께 생성된다는 뜻이다. 여러 p-tau 바이오마커가 동반 상승하는 이유를 조직 수준에서 설명해준다.
왜 Figure 1은 anti-Aβ 항체, Figure 2는 ThS를 사용했을까?
Figure 1 — anti-Aβ 항체 사용
목적은 Aβ plaque가 있든 없든, 어떤 형태든 모두 잡아서 p-tau217과의 공간적 관계를 보는 것이다. anti-Aβ 항체는 Aβ 펩타이드 자체에 결합하므로 diffuse든 dense-core든 모든 단계의 plaque를 검출할 수 있다. 채널 구성도 p-tau217(녹색) + Aβ 항체(마젠타) = 2채널이면 충분하다.
Figure 2 — ThS 사용
목적은 p-tau217, AT8, p-tau231 등 여러 p-tau 항체를 동시에 염색하면서 Aβ plaque도 표시하는 것이다. 형광 현미경의 채널 수에는 한계가 있고, 항체는 각각 1채널을 차지한다. p-tau217 + AT8 + anti-Aβ로 항체 3개를 쓰면 채널이 부족해진다. ThS는 항체가 아니라 화학 염색 시약이므로 항체 채널을 차지하지 않는다. 따라서 p-tau217(녹색) + AT8(마젠타) + ThS(시안) 이렇게 3채널을 효율적으로 사용할 수 있다.
즉, 채널 확보를 위한 실험 설계상의 선택이다. ThS를 쓰면 diffuse plaque는 놓칠 수 있지만, Figure 2의 관심사는 "성숙 plaque 주변에서 여러 p-tau가 공존하는가"이므로 ThS로 충분하다.
Results II: 세포 유형 및 시냅스 위치
p-tau181 축삭 변형, 시냅스 마커 공존, 글리아 non-engulfment
알아두면 좋을 것: 시냅스 구조와 글리아 세포
이 섹션에서는 p-tau217이 시냅스의 어느 쪽에 있는지, 글리아 세포가 이를 engulf — 세포가 대상을 통째로 감싸 삼키는 것 — 하는지를 분석한다. 관련 용어를 정리하면:
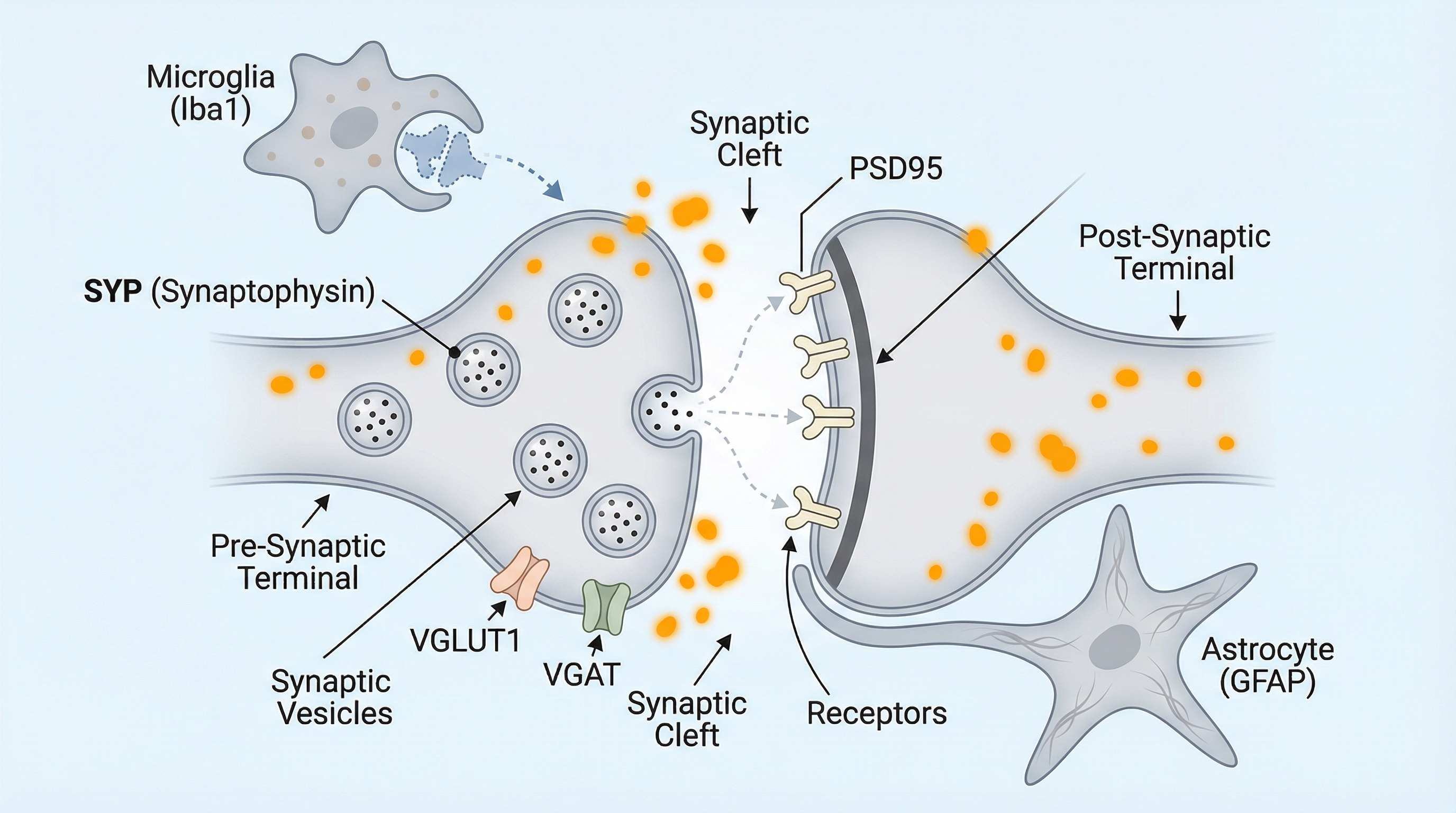
Pre-synapse — neurotransmitter vesicle이 있는 axon terminal. 마커: SYP(synaptophysin). 흥분성은 VGLUT1, 억제성은 VGAT으로 구분.
Post-synapse — receptor와 scaffolding protein이 있는 dendritic spine. 마커: PSD95.
Microglia — 뇌의 면역 세포. 마커: Iba1. 손상된 synapse를 engulf할 수 있다.
Astrocyte — 뉴런을 지지하는 glia. 마커: GFAP. 돌기가 synapse를 감싸며, synaptic engulfment에도 관여.
p-tau181: myelinated axon에 정상 존재, Aβ plaque 주변에서 변형
p-tau181의 축삭 분포
p-tau181은 정상적으로 myelinated axon — 글루타메이트성 흥분 뉴런과 GABAergic 억제 뉴런 모두 — 에 존재한다. 그러나 Aβ plaque 주변에서 p-tau181 양성 축삭과 myelin이 뒤틀리고 변형된다. preclinical AD에서 p-tau217 양성 puncta가 이 변형된 p-tau181 양성 축삭 주변에서 공존하며, p-tau262도 동일 부위에서 검출된다.
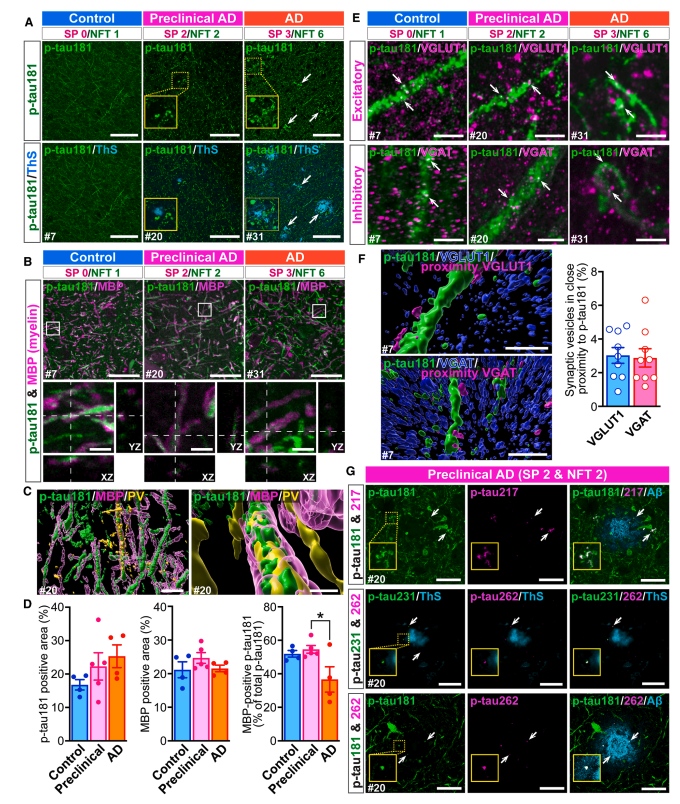
ThS, Thioflavin-S; MBP, myelin basic protein; PV, parvalbumin; VGLUT1, vesicular glutamate transporter 1; VGAT, vesicular GABA transporter. 클릭하여 확대
Figure 3 간단 요약: 이 그림이 왜 중요한가?
핵심 질문: p-tau217이 plaque 주변에 나타난다는 건 알겠다. 그런데 정확히 어떤 구조물에서 나타나는 건가? 축삭인가, 시냅스인가, 세포체인가?
이 Figure가 보여주는 것: 먼저 p-tau181이라는 '정상적으로 축삭에 있는' p-tau를 기준점으로 삼았다. p-tau181은 정상 뇌에서 myelin으로 감싸진 축삭을 따라 깔끔하게 분포한다. 그런데 Aβ plaque 주변에서 이 축삭들이 물리적으로 뒤틀리고, 바로 그 변형된 축삭 위에 p-tau217이 함께 나타난다. Aβ plaque가 주변 축삭을 손상시키고, 그 손상 부위에서 tau의 비정상 인산화가 일어나고 있다는 뜻이다.
p-tau217은 Pre- 및 Post-시냅스에 위치
시냅스 마커와의 공존
STED super-resolution 분석 결과, p-tau217은 pre-synapse marker SYP와 ~38%, post-synapse marker PSD95와 ~25% 공존. SYP와의 공존율이 유의하게 높음, *p<0.05 → p-tau217은 post-synapse보다 pre-synapse에 더 많이 위치.
글리아에 의한 engulfment 없음
microglia(Iba1+)에 의한 p-tau217 puncta engulfment는 0.005%로 PSD95(0.7%)보다 현저히 낮음. astrocyte(GFAP+)에 의한 engulfment도 0.4%로 SYP(3%)보다 유의하게 낮음(p<0.001). → p-tau217은 글리아 engulfment 대상이 아님.
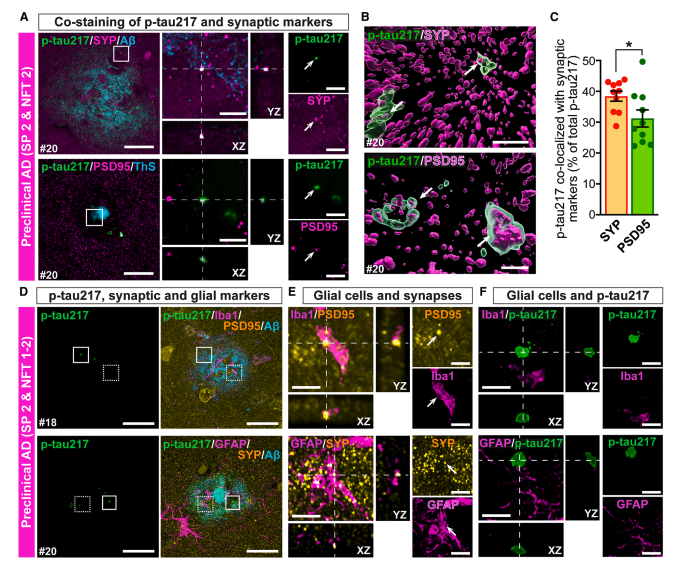
STED, stimulated emission depletion; SYP, synaptophysin; PSD95, post-synaptic density protein 95; ThS, Thioflavin-S; Iba1, ionized calcium-binding adapter molecule 1; GFAP, glial fibrillary acidic protein. 클릭하여 확대
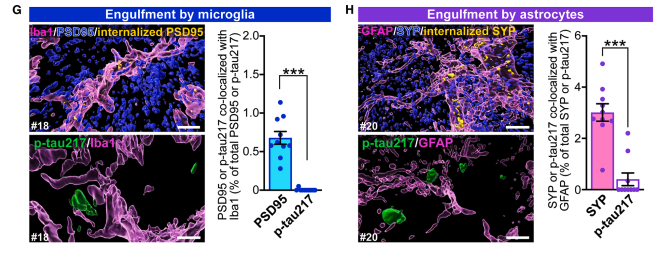
Iba1, ionized calcium-binding adapter molecule 1; PSD95, post-synaptic density protein 95; GFAP, glial fibrillary acidic protein; SYP, synaptophysin. 클릭하여 확대
Figure 4 D-F: Glia는 synapse를 먹지만, p-tau217은 안 먹는다
(D) 조감도 — p-tau217 + glia + synaptic marker + Aβ를 한 시야에 넣은 overview. 상단: p-tau217 녹색 + microglia Iba1 마젠타 + PSD95 노란 + Aβ 시안. 하단: p-tau217 녹색 + astrocyte GFAP 노란 + SYP 빨강 + Aβ 시안. Plaque 주변에서 이 네 가지가 공존하는 공간적 맥락을 보여준다.
(E) Glia가 synapse를 engulf하는 장면 — positive control — 직교 단면 YZ/XZ 확대. 상단: Iba1+ microglia 내부에 PSD95 신호가 들어가 있음 → microglia가 post-synapse를 삼킴. 하단: GFAP+ astrocyte 내부에 SYP 신호가 들어가 있음 → astrocyte가 pre-synapse를 삼킴. AD에서 glia의 synaptic engulfment가 실제로 일어나고 있음을 확인.
(F) 그런데 p-tau217은 glia 안에 없다 — 핵심 — 같은 직교 단면 방식. 상단: Iba1+ microglia 안에 p-tau217 신호 없음. 하단: GFAP+ astrocyte 안에도 없음. E에서 glia가 synapse를 활발히 삼키고 있는데도, p-tau217은 glia 내부에서 발견되지 않는다 → p-tau217 puncta는 glia가 삼킨 잔해가 아니라, 아직 살아있는 synapse에 존재.
Figure 4 G-H: Engulfment 정량 — 숫자로 확인
(G) Microglia engulfment — Iba1+ microglia 내부에서 검출되는 비율: PSD95는 ~0.7%가 검출되지만, p-tau217은 0.005%만 검출. ***p<0.001. Microglia가 PSD95(post-synapse)는 삼키지만 p-tau217은 거의 삼키지 않는다.
(H) Astrocyte engulfment — GFAP+ astrocyte 내부에서 검출되는 비율: SYP는 ~3%가 검출되지만, p-tau217은 ~0.4%만 검출. ***p<0.001. 패턴이 동일하다 — glia는 synaptic marker는 삼키지만 p-tau217은 선택적으로 회피.
D-F의 이미지 관찰을 정량적으로 뒷받침하는 패널. p-tau217이 glia engulfment의 산물이 아님을 통계적으로 확정한다.
Figure 4 간단 요약: 이 그림이 왜 중요한가?
핵심 질문: Figure 4A-C에서 p-tau217이 synaptic marker SYP·PSD95와 겹친다는 걸 확인했다. 그런데 현미경에서 "겹친다"는 두 가지로 해석된다:
(1) p-tau217과 SYP가 같은 살아있는 synapse 안에 있다 → synapse 자체에서 tau 인산화가 진행 중
(2) Glia가 synapse를 통째로 삼킨 뒤, glia 뱃속에 SYP 잔해와 p-tau217이 함께 들어있다 → synapse는 이미 죽었고, glia 내부에서 겹쳐 보이는 것
AD에서 microglia·astrocyte가 synapse를 engulf하는 건 잘 알려져 있으므로, (2)를 배제해야 (1)을 주장할 수 있다.
Figure 4D-H가 보여주는 것: Glia는 synaptic marker(PSD95, SYP)를 실제로 engulf하고 있다 — 이건 사실이다(E). 그런데 같은 glia 안에서 p-tau217은 거의 발견되지 않는다(F, G, H). 즉 glia가 synapse를 삼킬 때 p-tau217은 따라 들어가지 않는다. p-tau217은 glia에게 먹힌 synapse 잔해가 아니라, 아직 glia에게 먹히지 않은 살아있는 synapse에 존재하는 것이다.
Results III: 뉴런 유형 및 Tau Kinase
흥분/억제 뉴런 모두에서 출현, 활성 kinase와 공존
알아두면 좋을 것: Tau kinase란?
Kinase는 단백질에 phosphate group을 붙이는 효소이다. Tau의 특정 부위를 인산화하는 kinase를 tau kinase라 부른다. 이 섹션에서 다루는 3가지:
GSK3β (Glycogen Synthase Kinase 3β) — AD 연구에서 가장 주목받는 tau kinase. Tau의 여러 부위(Thr181, Thr217 포함)를 인산화할 수 있다. AD 뇌에서 활성이 증가하며, 치료 표적으로 연구 중.
Cdk5 (Cyclin-Dependent Kinase 5) — 정상적으로 뉴런 발달에 관여하지만, AD에서 p25라는 비정상 활성화 인자와 결합하면 tau를 과인산화시킨다.
JNK (c-Jun N-terminal Kinase) — 스트레스 반응 kinase. 산화 스트레스, Aβ 독성 등에 의해 활성화되며 tau를 인산화한다.
이 세 kinase 모두 in vitro에서 tau의 Thr217 부위를 인산화하는 것이 확인되어 있다. 이 섹션에서는 이들이 실제로 preclinical AD 뇌의 시냅스에서 p-tau217과 함께 존재하는지를 검증한다.
흥분성 + 억제성 뉴런 시냅스 모두에서 p-tau217 출현
NFT vs p-tau217의 뉴런 유형 차이
AD 뇌에서 NFT(AT8+)는 주로 흥분성 뉴런 마커 SATB2와 공존하고 억제성 마커 GAD67과는 거의 공존하지 않음. 이는 NFT가 선택적으로 글루타메이트성 흥분 뉴런에서 형성됨을 의미.
p-tau217: 뉴런 유형 비선택적
반면, preclinical AD에서 p-tau217은 흥분성 마커 VGLUT1과 ~20%, 억제성 마커 GAD67과 ~15% 공존. NFT와 달리 p-tau217은 두 유형 뉴런 시냅스 모두에서 나타남 → NFT 형성과 독립적인 메커니즘 시사.
p-tau217 양성 시냅스에 활성 Tau Kinase 농축
Thr217 인산화를 촉매하는 kinase
Tau의 Thr217 부위는 proline-directed kinase의 기질이다. GSK3β(glycogen synthase kinase 3β), Cdk5(cyclin-dependent kinase 5), JNK(c-Jun N-terminal kinase)이 in vitro에서 Thr217을 인산화하는 것이 알려져 있다. 본 연구에서는 이 세 kinase가 preclinical AD 뇌의 Aβ plaque 주변 p-tau217 양성 시냅스에 공존하는지 조사하였다.
- GSK3β: p-tau217 양성 puncta의 ~30%가 활성 GSK3β와 공존. Pre-시냅스(SYP+) 내에서는 ~52%로 가장 높은 공존율
- Cdk5: p-tau217의 ~17% 공존. Pre-시냅스 내 ~27%
- JNK: p-tau217의 ~20% 공존. Pre-시냅스 내 ~36%
- p-tau217 양성 pre-시냅스는 총 SYP 대비 각 kinase와 유의하게 높은 공존율 → p-tau217 시냅스에 활성 kinase가 농축
- GSK3β가 가장 강하게 공존하며, preclinical AD pre-시냅스에서 kinase 활성이 유의하게 상승(p<0.05, p<0.01)
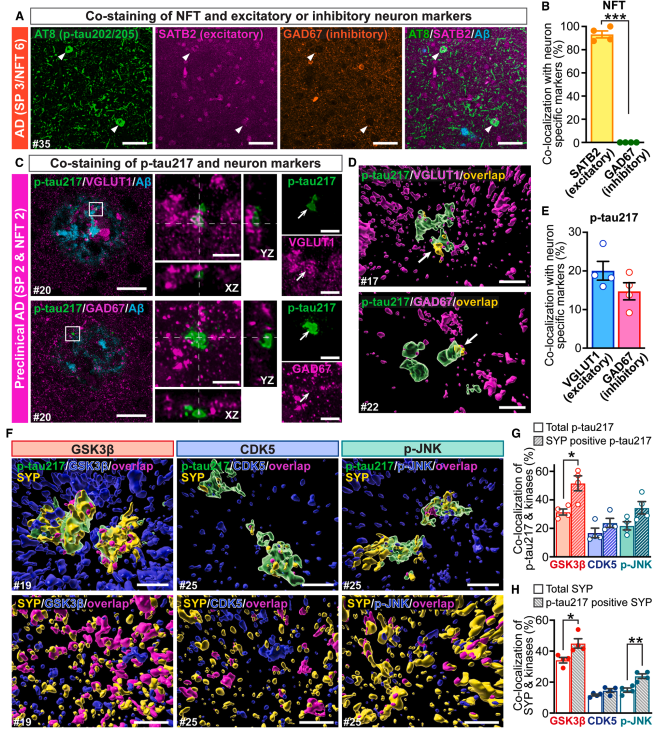
AT8, anti-p-tau202/205; SATB2, excitatory neuron marker; GAD67, inhibitory neuron marker; VGLUT1, vesicular glutamate transporter 1; SYP, synaptophysin; GSK3β, glycogen synthase kinase 3β; Cdk5, cyclin-dependent kinase 5; JNK, c-Jun N-terminal kinase. 클릭하여 확대
Figure 5 간단 요약: 이 그림이 왜 중요한가?
핵심 질문 1: AD에서 NFT는 주로 흥분성 뉴런에서만 생긴다. p-tau217도 마찬가지인가?
답: 아니다. NFT(AT8)는 ~90%가 흥분성 뉴런(SATB2+)에서만 검출되지만, p-tau217은 흥분성(VGLUT1, ~20%)과 억제성(GAD67, ~15%) 시냅스 모두에서 나타난다. p-tau217은 NFT와 다른 메커니즘으로 생성된다는 뜻이다.
핵심 질문 2: 그렇다면 p-tau217은 어떻게 만들어지는 건가? 그냥 수동적으로 떨어져 나온 건가?
답: 아니다. p-tau217 양성 시냅스에는 tau를 인산화하는 효소(GSK3β, Cdk5, JNK)가 정상 시냅스보다 유의하게 많이 모여 있다. 특히 GSK3β는 p-tau217 양성 pre-시냅스의 52%에서 검출된다. 시냅스 안에서 kinase가 능동적으로 tau를 인산화하고 있다는 직접 증거이다.
이 결과는 혈장 p-tau217이 단순히 뉴런 사멸의 부산물이 아님을 보여준다. 살아있는 시냅스에서 kinase에 의해 능동적으로 만들어지는 것이다. 따라서 p-tau217 수치 변화는 neurodegeneration보다는 synaptic dysfunction(시냅스 기능 이상)의 초기 지표로 해석하는 것이 더 적절하다. GSK3β 억제제 등 kinase 표적 치료의 근거도 될 수 있다.
Discussion
p-tau217 바이오마커의 신경병리학적 해석과 임상적 함의
바이오마커 해석: Aβ에 대한 시냅스 반응
혈장 p-tau217이 preclinical AD에서 Aβ 축적을 반영한다는 기존 관찰에 대해, 본 연구는 뇌 조직 수준에서의 해석을 제공한다. p-tau217은 Aβ plaque 주변 시냅스에서 능동적 kinase 활성을 통해 생성되며, glial engulfment가 아닌 뉴런/시냅스의 직접적 반응을 반영한다.
항-Aβ 면역요법과의 연결
최근 개발된 항-Aβ 면역요법(aducanumab, lecanemab 등)에서 Aβ plaque 제거 시 혈장 p-tau217이 감소한다. 본 연구 결과는 이 현상을 설명: Aβ plaque가 줄면 주변 시냅스의 이상 tau 인산화 반응도 감소하기 때문이다.
p-tau217 vs p-tau181: 서로 다른 의미
p-tau217은 Aβ plaque 주변 시냅스의 이상 반응을 반영하는 반면, p-tau181은 축삭 손상의 지표이다. p-tau181은 myelinated axon에 정상 존재하며 Aβ 주변에서 axon이 변형될 때 방출된다. 따라서 두 바이오마커는 서로 다른 병리생리학적 과정을 반영할 수 있다.
NFT 형성과의 독립성
NFT는 주로 흥분성 뉴런에서 선택적으로 형성되지만, p-tau217은 흥분성 및 억제성 뉴런 시냅스 모두에서 나타난다. 이는 시냅스 내 p-tau217 출현이 NFT 형성과 독립적인 과정일 수 있음을 시사하며, p-tau217이 Aβ 매개 시냅스 기능 이상의 초기 지표가 될 수 있다.
p-tau217은 preclinical AD에서 Aβ plaque에 대한 뉴런/시냅스의 능동적 반응을 반영하는 바이오마커이다. glial engulfment가 아닌 시냅스 내 활성 kinase에 의한 tau 인산화가 그 기전이며, 이는 tau tangle 형성과 독립적으로 발생한다. 향후 항-Aβ 면역요법 환자의 CSF/혈장 샘플과 부검 뇌 조직을 연계한 검증 연구가 필요하다.